
1 : Classification, anatomie - 2 : Nutrition, reproduction - 3 : Écologie - 4 : Maintenance
1. Modèles de distribution - biotopes
Les Octocoralliaires occupent toutes les régions du globe. Ils sont plus nombreux dans la ceinture tropicale et la richesse des récifs coralliens augmente en se rapprochant de l’équateur et du centre de diversité (le triangle corallien : Philippines - Papouasie - Indonésie). Sessiles, ils sont soumis aux conditions environnementales (lumière, flux marins, sédimentation…) des lieux où leur larve s‘est implantée. Les préférences et la marge de tolérance des coraux varient de manière importante selon les espèces, certains ne supportent que quelques variations des conditions environnementales à la différence d’autres plus résistants aux perturbations. Ainsi la distance à la côte mais aussi la profondeur (et par corrélation, l'hydrodynamisme, la lumière, la turbidité et l'apport d'eau douce) sont reconnues pour être des facteurs structurant la présence ou l'absence de certaines espèces. Cependant de nombreux autres points sont très probablement à prendre en compte sans qu’ils aient toutefois été identifiés à ce jour.
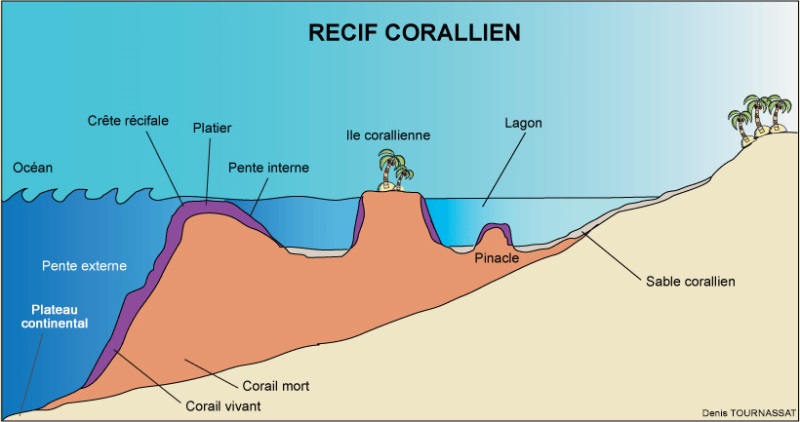
Les eaux des pentes continentales des récifs de la Grande barrière de corail, des atolls perdus au milieu des océans ou les eaux profondes de la Mer rouge sont claires, pauvres en particules, avec peu de dépôts sédimentaires, sans perturbation due aux écoulements côtiers avec occasionnellement, la remontée de nutriments issus des eaux profondes (upwelling). Dans ces habitats, les espèces zooxanthellées prolifèrent jusqu’à 20 m de profondeur. Les populations sont par contre plus faibles et les espèces moins nombreuses à l’approche des crêtes récifales, du fait de la vigueur des vagues, surtout sur les côtes situées au vent. On n’y trouve que de petites colonies telles que Xenia et Paralemnalia, ces conditions ne se prêtent pas au développement des espèces plus grandes comme Lemnalia ou Nephtea et la plupart des gorgones. Les gorgones apprécient mieux les zones exposées aux courants et à l’abri des vagues, à l’intérieur du récif ou en bas de la pente récifale.
Les conditions sont plus variées et les types d’habitats plus nombreux sur les récifs frangeants ou les récifs barrière (cf. Les récifs coralliens tropicaux). La densité des populations évolue selon la profondeur et la distance. On dénombre peu de colonies et d’espèces zooxanthellées dans les récifs proches de la côte aux eaux turbides dont la visibilité n’excède pas 2 m. Les Briareum et Sinularia pourront dominer dans les zones peu profondes tandis qu’on trouvera des gorgones azooxanthellées en bas du récif. Un peu plus loin de la côte ou la visibilité est de 2 à 5 m, on peut trouver des colonies de Clavularia, Briareum ainsi que quelques Sinularia, Sarcophyton et Klyxum. Alcyoniidés, Nephtéidés et Xeniidés domineront dans les eaux plus claire dont la visibilité est de l’ordre de 5 à 8 m. Ils pourront couvrir jusqu’à 70 % de l’espace dans des zones exposées aux courant à l’abri des vagues, laissant peu de place aux Scléractiniaires. Bien qu’ils occupent une faible surface, souvent inférieure à 5 %, les récifs occupant la zone photique, hébergent la plus grande diversité d’espèce d’Octocoralliaires. On y trouve des espèces côtières et parfois des espèces inféodées seulement à ce milieu.
2. Environnement physique
2.1 Tempêtes et vagues

Les cyclones et tempêtes génèrent des déplacements d’eau importants. Non seulement les houles chargées de sable abrasent et délogent les communautés d’Octocoralliaires mais leurs effets indirects comme les précipitations abondantes à l’origine de crues, du lessivage des sols ou des sédimentations, peuvent avoir des effets destructeurs sur les récifs.
Est-ce dû à leur relative souplesse ? Ces conditions cycloniques extrêmes détruisent finalement de relativement petites surfaces d’Octocoralliaires. Les zones les plus exposées sont occupées par des espèces résistantes et les espèces des zones mieux protégées supportent assez bien des conditions sévères.
Les crêtes récifales exposées au quotidien au vent à une forte action des vagues restent le domaine des coraux durs. Seules quelques espèces d’Octocoralliaires épais et encroûtants comme Sinularia, Cladiella et des espèces compactes comme Capnella, Paralemnalia, Asterospicularia et Xenia peuvent supporter ces conditions, à l’abri des failles ou derrière la zone déferlante. La plupart prolifèrent dans les zones moins exposées, comme les gorgones qui préfèrent les zones protégées ou les pentes raides côtoyant des courants. Beaucoup de N ephtéidés se protègent des déchirures, durant les orages, en contractant fortement la colonie mais on ne les voit jamais dans des zones exposées.
2.2 Courants
Les Octocoralliaires n'occupent pas seulement les zones relativement protégées des lagons. Leur habitat se prolonge sur la pente récifale jusqu'à des profondeurs importantes. On les trouve en nombre, accrochés aux parois des passes, entre îles et îlots et sur les tombants abrupts. Ces milieux sont balayés par des courants unidirectionnels souvent très puissants. Ils transportent la nourriture, évacuent les déchets plus au loin et stimulent la respiration. Les gorgones azooxanthellées sont habituellement placées perpendiculaires au courant pour mieux intercepter les particules de nourriture. Plutôt horizontales ou verticales, les morphes de croissance des espèces zooxanthellées, sont un compromis entre la capture de nourriture et l'exposition à la lumière. Courants et lumière, ce sont bien là deux paramètres essentiels.
2.3 Lumière

La répartition des Octocoralliaires varie en fonction de l’exposition à la lumière, qui dépend de la profondeur, de la clarté de l’eau, de l’inclinaison, de la conformation de la pente récifale. Si les Scléractiniaires s'imposent souvent au sommet du récif, le ratio Scléractiniaires / Octocoralliaires évolue en faveur de ces derniers avec la profondeur. Mais ce n'est pas non plus une règle absolue.
La modification de l’indice de réfraction engendré par des pluies abondantes qui forment une couche superficielle, tout comme les particules en suspension, non seulement sont responsables de la turbidité mais absorbent la lumière. Une eau turbide à 10 mètres de profondeur peut déjà être sombre en milieu de journée. La turbidité est plus importante dans les faibles fonds de la pente continentale du récif proche de la côte ou des embouchures où les vagues et les marées remettent en suspension les sédiments et la vase.
Le rayonnement solaire agit directement sur le taux de la photosynthèse. La lumière active la croissance des espèces zooxanthellées, a contrario elle repousse beaucoup d’espèces non photosynthétiques dont les larves se fixent préférentiellement dans les zones sombres. La profondeur limite acceptable pour les coraux augmente avec la clarté de l’eau : dans les zones turbides elle est de 10 mètres pour les espèces zooxanthellées et en deçà les espèces azooxanthellées prédominent (Ellisidés, Subergorgiidés, gorgones Plexauridés et Dendronephthya). Dans les eaux claires, quelques espèces photosynthétiques (Sinularia) croissent jusqu’à 40 mètres de profondeur, les espèces azooxanthellées débutant dans la zone des 25 mètres. La lumière est également faible dans les pentes raides et les tombants propices aux espèces peu exigeantes comme Briareum, Sinularia et les azooxanthellés.
Les Octocoralliaires n’occupent pas exactement les mêmes niches écologiques que les Scléractiniaires pour deux raisons essentielles : leur faible aptitude à chasser avec leur cnidocytes associée à la petitesse des particules de leur nourriture picoplanctonique et puis leur forte biomasse ne permet pas la transmission de la lumière autant que la finesse des tissus de nombreux sps, chez lesquels la photosynthèse est plus efficace. Dans le milieu naturel, on ne constate donc pas de véritable concurrence pour la lumière avec ces derniers.
2.4. Nutriments
Les nutriments particulaires et dissous proviennent de sources très différentes dans les eaux océaniques et eaux côtières. Les eaux océaniques tropicales sont claires, appauvries par la croissance planctonique associée aux processus de dégradation. Cependant l’upwelling remonte les eaux froides du fond, enrichies en nutriments, jusqu'aux pentes continentales des récifs. Ce courant ascendant augmente significativement les concentrations de matières dissoutes dans les eaux de surface, bien que leurs fréquences et étendues varient considérablement d’une région à l’autre. Ces zones sont souvent dominées par des coraux mous comme les Xeniidés qui absorbent ces nutriments dissous.
Les eaux côtières peu profondes, en raison de l'écoulement terrestre et la remise en suspension des sédiments, ont des concentrations alimentaires plus variables et souvent supérieures à celles du large propres à la prolifération du phytoplancton et la croissance de micro-organismes. De telles zones ont tendance à être dominées par les coraux mous Alcyoniidés à faible profondeur du fait de la faible pénétration de la lumière.
Malheureusement, dans de nombreuses régions tropicales, les rejets d'eaux usées, les ruissellements chargés d’engrais et de pesticides issus du déboisement et de l’agriculture, contribuent au déclin des écosystèmes côtiers et ce jusqu’à des dizaines de kilomètres au large. La plupart des Octocoralliaires sont absents de ces zones polluées et les gorgones azooxanthellées habituellement moins sensibles à ces pollutions, subissent un taux de mortalité plus élevé à cause d’infections fongiques et/ou bactérienne mais aussi par compétition (colonisation par les algues, balanes, bryozoaires, anémones).
2.5. Sédimentation

La sédimentation est une cause importante de dégradation des récifs à l’échelle mondiale. Elle varie de manière naturelle sur les récifs mais elle est également associée aux actions humaines, de nature à détruire le couvert végétal. La déforestation, le traitement chimique des terres agricoles, l’urbanisation du littoral, les exploitations minières et les travaux de terrassement environnants, génèrent de profondes modifications du profil littoral et la dégradation des récifs frangeants. Les sédiments drainés par les rivières sans retenue conduisent à l’eutrophisation du milieu et s’avèrent néfastes sur la santé des récifs coralliens, surtout si elle se combine avec des taux élevés de nutriments comme c'est souvent le cas dans les zones exposées à des eaux de ruissellement agricoles.
Les dépôts de sédiments obstruent les pores des tissus et étouffent les coraux notamment les petites colonies et les juvéniles en limitant les échanges gazeux avec l’eau. Ils occasionnent un stress chez le corail et réduisent la photosynthèse en raison de l'absorption de la lumière par les particules déposées sur les colonies ou celles en suspension dans l'eau.
Une étude sur la Grande barrière de corail, montre que le taux de sédimentation augmente avec la profondeur et le rapprochement de la côte. La valeur maximale a été mesurée sur fond de 10 mètres au niveau du plateau intérieur du récif. La tolérance des Octocoralliaires varie considérablement selon les espèces. De nombreuses, en particulier les Xeniidae et Nephtheidae, se limitent aux eaux relativement claires alors que la plupart des Alcyoniidae (Sinularia, Sarcophyton, Lobophytum, et Klyxum) conservent une croissance rapide et importante dans les zones côtières turbides, modérément éclairées. Par contre les gorgones azooxanthellées (Ellisellidae, Subergorgiidae) abondent dans des zones troubles, même en eau peu profonde. Peut-être en raison du champ libre laissé par les autres coraux du fait du peu de clarté associée à une turbidité élevée et une forte sédimentation.
2.6. Salinité
| Localisation | Salinité |
|---|---|
| Eaux douces continentales | 0 à 0.5 |
| Atlantique nord | 30.0 |
| Océan Pacifique | 35.0 |
| Océan indien | 36.5 |
| Océan Atlantique | 36.5 |
| Mer Méditerranée | 38.5 |
| Mer rouge | 39.7 |

On sait peu de chose sur le niveau de tolérance des espèces aux variations de salinité. La salinité moyenne des océans est à peu près stable, 35 en Indopacifique, et plus élevée dans les mers fermées, jusqu’à 45 dans le nord de la Mer Rouge et dans le Golfe Persique. L’augmentation de la salinité de 2 à 3 due à l’évaporation n’est, en principe, pas un problème. Cependant, la baisse de salinité sur les platiers durant la mousson peut être préjudiciable. En présence d’eau de mer diluée, la chute de différence de pression osmotique de part et d’autre des membranes cellulaires aboutit à des perturbations physiologiques importantes, pouvant aller jusqu’à la mort des coraux. Une salinité inférieure à 30 semble préjudiciable en particulier pour de nombreux Xeniidés, et des valeurs inférieures à 25 sont mortelles pour la plupart des espèces.
2.7. Température
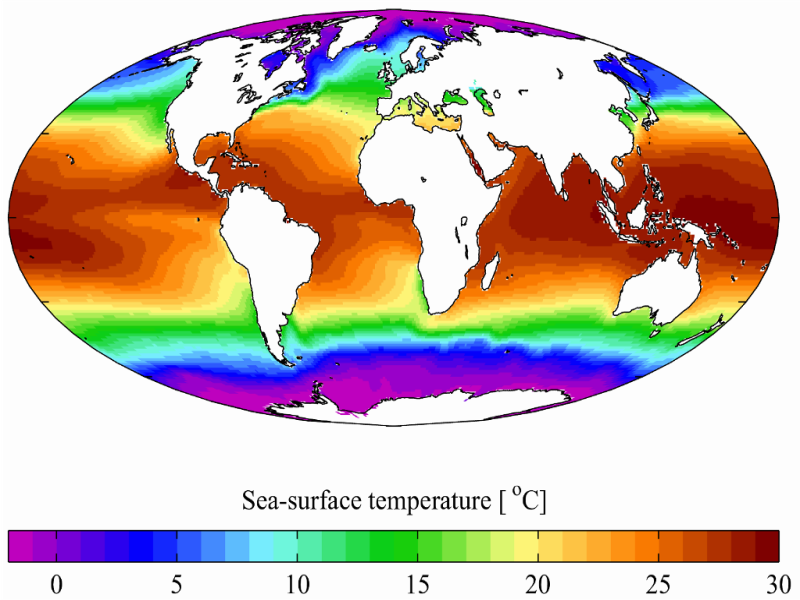
Les Octocoralliaires peuplent quasiment toutes les mers du globe. Les espèces tropicales se répartissent entre les deux tropiques, là où les larves planctoniques sont portées, d’est en ouest, par les courants superficiels et chauds (illustrations).
Les espèces photo symbiotiques se développent dans les eaux dont la température est adaptée à la marge de tolérance étroite de leurs algues symbiotiques et essentiellement dans les eaux de surface où les moyennes de températures oscillent autour de 25°C. La température limite supérieure acceptable varie selon les régions, mais avoisine 31°C, seules quelques espèces peuvent supporter des pointes extrêmes épisodiques à 34°C mesurées localement sur des platiers ou dans des baies protégées du vent.
Les espèces zooxanthellées se font plus rares quand la température descend durant de longues périodes en dessous de 18°C.
Les espèces azooxanthellées sont en mesure de prospérer dans les eaux tropicales plus profondes au-delà de 40 m et celles tempérées ou froides jusqu'à 4°C. Leur résistance est propre à l’espèce mais aussi à ses caractères génétiques, elle n’a pas fait l’objet de publication mais, les températures des eaux de fond étant plus stables, on peut imaginer qu’elles supportent moins les dérives.


Il suffit d’une hausse de un à deux degrés au-dessus de la moyenne maximale estivale pour provoquer l'expulsion des zooxanthelles des organismes photosynthétiques, engendrant le blanchissement du corail. (photo). La température souvent trop élévée et parfois trop basse est la cause principale des blanchissements soudains, mais d’autres facteurs de stress peuvent le provoquer, tels que des infections bactériennes, l'eau douce, les sédiments, la surexposition à la lumière ultraviolette ou visible. La population de zooxanthelles peut se rétablir dans la colonie si la cause du stress cesse après une courte période. Toutefois, si le stress est sévère ou persiste trop longtemps, les organismes meurent. Les chances de survie varient selon les espèces, les Xeniidés périssent en quelques jours, les Nephtéidés semblent moins sensibles, les Alcyoniidés résistent mieux et peuvent survivre durant des mois.

Les événements de blanchissement de masse ont augmenté au cours des dernières décennies et sont clairement liés aux changements climatiques. Les concentrations de dioxyde de carbone dans l'atmosphère entraînent un "effet de serre" et une augmentation des températures maximales sous les tropiques. Elles constituent l'une des plus de graves menaces pour la santé des récifs coralliens, ne sachant pas si les coraux pourront s'acclimater à ce réchauffement océanique.
2.8. Perturbations anthropiques
Les perturbations naturelles occasionnent des dégâts sur les récifs mais sans engendrer des effets néfastes à long terme. Au contraire, ils permettent aux espèces les moins compétitives de reconquérir des territoires. Les grands fléaux ne peuvent survenir qu’à la suite du renouvellement de perturbations. Les coraux adultes étant plus résistants, ils retardent le constat de l’ampleur des détériorations, parfois après des années. La diminution de certaines espèces de coraux du fait de ces perturbations, n’est en général pas compensée par l’installation d’autres espèces ; les envahisseurs comme les algues ont tôt fait de prendre le dessus et de réduire la diversité des espèces en conséquence.
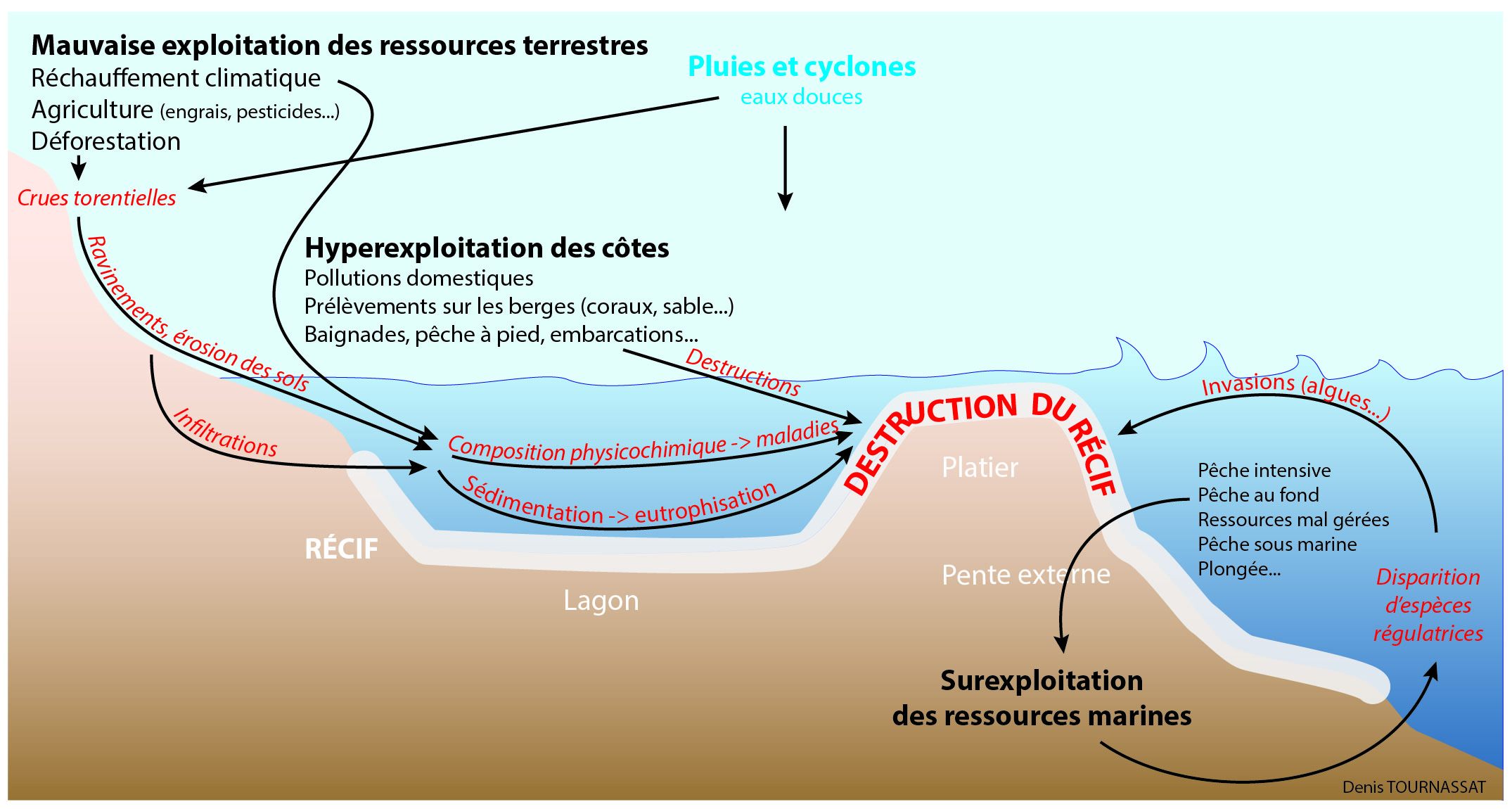
Les principales causes de la mort des récifs sont le fait des activités humaines et de leurs répétitions (illustration) :
- Mauvaise exploitation des ressources terrestres : déforestation générant des écoulements rapides vers la mer, sources de sédimentation et d’eutrophisation des fonds ; utilisation de traitements agricoles (engrais, pesticides) sources d’enrichissement en phosphates, nitrates ; réchauffement climatique qui découle de nos pollutions avec ses effets sur la température et l’acidification des océans.
- Hyper exploitation des côtes : activités de loisirs, constructions, ports et amarrages inadaptés… ; pollution urbaine et industrielle qui draine des hydrocarbures, détergents et métaux lourds.
-
Surexploitation des ressources marines : pratiques de pêches destructrices (explosifs, cyanure, chaluts) qui affectent directement les organismes de fond ; mauvaise gestion des ressources orientée sur certaines espèces ; diminution des prédateurs puis des herbivores qui laissent proliférer les macroalgues au détriment des communautés coralliennes.
3. Ecologie, protections, défenses et agressions chimiques, physiques, biochimiques
Les Octocoralliaires sont sessiles et ne peuvent donc pas se cacher ou fuir face aux dangers, qu’ils soient d’origines physicochimiques humaines ou naturelles, provenant de parasites, de prédateurs (coraux, éponges, algues, gorgones, anémones) ou de concurrents. Pour conserver une bonne place sous la lumière ou dans le flux des nutriments apportés par le courant, ils ne sont pas sans défenses et sont capables de synthétiser des substances chimiques (métabolites secondaires) en mesure de se protéger des envahisseurs ou des rayonnements solaires nocifs, de dissuader des prédateurs ou même d’agresser d'autres invertébrés. Les moyens de protection des Octocoralliaires s'avèrent d'ailleurs plutôt efficaces puisque qu'on ne constate pas chez eux des mortalités à grande échelle dues à des prédations comme dans le cas des Scléractiniares avec l'étoile de mer Acanthaster planci.
3.1. Substances antiappétantes contre la prédation
Les substances chargées de dissuader les prédateurs sont toxiques ou plus simplement, réduisent l'appétence. La plupart appartiennent à un groupe de composés chimiques les terpénoïdes. De nombreuses espèces de coraux les produisent et les stockent au stade larvaire ou adulte. Ces substances sont efficaces contre la plupart des prédateurs mais quelques-uns, comme la porcelaine Ovula ovum prédatrice des Alcyonacés qui broute à la surface des colonies, ont développé génétiquement une aptitude à décomposer ces toxines par des processus métaboliques. D'autres espèces, comme Dendronephthya hemprichi de Mer Rouge qui dispose d’un faible niveau de protection chimique contre la prédation, compensent leurs pertes élevées dues aux brouteurs (escargots Ovula et Drupella, oursin Diadema et les Poissons-papillon), par des taux de croissance et de reproduction rapides.
On observe sur les Alcyoniidés et parfois sur Efflatounaria, de nombreuses cicatrices laissées par de grands prédateurs. C'est moins le cas pour les autres espèces, soit parce qu'elles guérissent plus vite ou au contraire parce qu’elles sont plus sensibles et meurent des suites de leurs blessures sans laisser de preuve. Certaines demoiselles (Neoglyphidodon melas) et poissons-papillons (Chaetodon melanotus, C. fasciatus, C. paucifasciatus) se nourrissent d’Octocoralliaires par la cueillette sélective de polypes individuels, sans causer de dommages significatifs aux colonies. Certains nudibranches appartenant aux familles des Arminidae : Dermatobranchus ; des Dendronotidae: Tritonia et Tritonopsilla et des Aeolididae : Phyllodesmium, se nourrissent exclusivement de coraux mous et de gorgones. Ils sont souvent mimétiques au niveau de la couleur et de la forme de leur proie ou hôte. Ces nudibranches, ingèrent non seulement les tissus de l’Octocoralliaire mais également ses zooxanthelles pour assurer leur propre énergie par la photosynthèse. Ils assimilent également les pigments de leur proie pour améliorer leur camouflage. Acanthaster planci la redoutable étoile de mer prédatrice de coraux durs, mange rarement des Octocoralliaires et reste sans effet sur les populations.
La faculté des Octocoralliaires à guérir et régénérer leurs branches perdues en raison de la prédation, est largement exploitée pour la production de boutures en aquariophilie récifale. Les branches d’une colonie peuvent être simplement coupées et fixées sur un nouveau substrat pour former une nouvelle colonie.
3.2. Interactions avec d'autres espèces, symbiose
De nombreux animaux exploitent la protection des Octocoralliaires et vivent sur leur partenaire de manière temporaire ou permanente. Les plus visibles sont les balanes, les moules et les crinoïdes qui se perchent sur les gorgones pour une meilleure exposition aux courants. On trouve également, régulièrement associés aux Octocoralliaires, des Gobiesocidae, des hippocampes, des ophiures, des cténophores, des escargots, des vers, des crevettes, des crabes et d’autres crustacés comme les copépodes. Ces associations présentent plusieurs intérêts depuis, le refuge jusqu’au garde-manger en consommant le mucus ou le tissu des Alcyonacés. Ces épibiontes (qui vivent sur leur hôte) sont souvent bien camouflés, imitant la coloration et le pattern de leur hôte. On trouve également fréquemment des algues épiphytes accrochées à la base des Octocoralliaires.



Cependant, il est bien souvent impossible de déterminer si ces associations sont de type symbiose mutualiste (relation bénéfique réciproque) puisque les animaux hébergés peuvent par exemple déparasiter leurs hôtes, voire le protéger de certains prédateurs, de type symbiose commensale (l'hôte fournit la nourriture, mais ne subit pas de préjudice important), ou symbiose parasite (l'hôte subit des dommages, mineurs ou pouvant entrainer la mort).
3.3. Substances pesticides et nettoyantes
Substances bioactivesLes chercheurs s'intéressent aux substances secrétées par les Octocoralliaires et d’autres invertébrés (éponges, ascidies…). Ils ont identifié des sesquiterpènes (Calaménènes), diterpènes (Désoxyhavannahine, Lobophynine, Eunicelline, Flexibilide), stéroïdes (Litostérol), polyamine, caroténoïdes, phénols, alcaloïdes, peptides, sinulolides, buténolides (furanone)... aux propriétés ciblées et parfois multiples (défense, antibactérienne, anti-inflammatoire, cytotoxique). Ainsi Dendronephthya secrète des stéroïdes (isogosterones) et Sinularia sp., des composés de types sinularones (cyclopentenone, furanone) et buténolides aux propriétés antifouling. L'Alcyoniidé Cladiella et les gorgones Eunicea et Astrogorgia, libèrent des diterpénoïdes de type Eunicelline et des stérols antifouling, anti-inflammatoires et antibactériens. La Désoxyhavannahine libérée par Xenia est un antibactérien très efficace... La liste ne fait que grandir !
Certaines substances bioactives, pesticides, parfois nommées "antifouling" ou "antisalissure", empêchent l'installation et la croissance sur le corail, d'organismes nuisibles (algues, champignons, bactéries et autres colonisateurs potentiels). Une colonie qui perd temporairement ou définitivement sa protection, est rapidement sujette aux infections occasionnées par l'encrassement des tissus. La perte de ces substances semble souvent liée à des stress environnementaux graves tels que la pollution, la sédimentation ou une température élevée. Les colonies stressées et affaiblies ne peuvent détourner l’énergie nécessaire aux processus métaboliques vitaux pour la production de ces substances qui en exigent également beaucoup.

C’est le cas des Alcyoniidés et des gorgones sujets aux invasions algales. Les gorgones ne guérissent pas à ces infections et on peut observer les branches mortes ou des portions, durant des mois, envahies par les algues et d'autres organismes. En revanche, certains Alcyoniidés plus persistants semblent en mesure de renforcer leur protection chimique et récupérer en quelques semaines à quelques mois.
Certaines substances conduisent à la formation d'un film cireux que les Octocoralliaires exfolient périodiquement pour nettoyer leur surface encrassée par des sédiments ou des organismes vivants. Cette "mue", comme la nomment les aquaripohiles dans leur jargon, est particulièrement importante sur les Alcyoniidés massifs tels que les coraux cuir comme Sarcophyton, Lobophytum. Mais on l'observe sur quantité d'espèces, sur les Nephtéidés Dendronephthya ou sur les branches de certaines gorgones Pterogorgia. Ce film, rapidement colonisé par des algues et qui peut être pris au départ pour une invasion est, en quelques jours, emporté par les courants laissant derrière lui des tisus propres.
3.4. Substances allélopathiques et lutte pour l’espace
De nombreuses espèces de coraux Scléractiniaires et Octocoralliaires doivent régulièrement dépenser leur énergie dans la lutte contre leurs voisins proches pour conserver, sinon agrandir, le territoire qui convient à leur prospérité. On l’a vu dans Octocoralliaires 1, ces coraux sont pourvus de cnidocytes mais petits et trop inefficaces pour mener une lutte rapprochée. Dans la pratique ils ne les utilisent pas sauf Erythropodium caribaeorum, seul Octocoralliaire des Caraïbes connu pour exploiter ses tentacules urticants.
Ces substances bioactives élaborées par les Octocoralliaires, à des fins de protection et de défense, ne laissent pas indifférents les laboratoires pharmaceutiques et les biochimistes, toujours à la recherche de nouveaux produits, et prêts à investir des budgets considérables pour leur extraction. Par exemple, des produits de soins utilisent les extrémités à croissance rapide des branches de la gorgone Pseudopterogorgia elisabethae et P. acerosa pour des composants diterpènes anti-inflammatoires. Ce marché offre plus en retour, aux populations locales, que la pêche à la dynamite et peut potentiellement contribuer à la conservation des récifs, pour autant qu’il soit éco responsable.
Les Octocoralliaires utilisent parfois la stratégie du recouvrement pour nuire à un adversaire, mais dans des habitats spécifiques et sans jamais établir une vraie hiérarchie. D’une manière générale, les compétiteurs stoppent leur croissance au contact du concurrent, la plupart des coraux mous sont d’ailleurs trop petits pour recouvrir leurs voisins hermatypiques. Leur guerre est plutôt chimique.

Leur stratégie consiste à inhiber la croissance et la survie des voisins par la libération lente et continue de substances chimiques dans l'eau (substances également utilisées pour le nettoyage, contre l’envahissement ou les prédateurs). Ce processus de défense chimique, l’allélopathie, est très efficace contre les Scléractiniaires. S'ils cohabitent souvent, il devient très difficile aux coraux durs de s'implanter quand l'espace est fortement colonisé par les espèces massives (coraux cuirs) en mesure de libérer de grandes quantités de toxines, notamment dans des zones moins brassées. Cette situation est particulièrement remarquable au sein des espèces symbiotiques. La cohabitation est meilleure, dans les zones ou le courant est aussi un vecteur de nutrition, ce dernier contribuant également à disperser les éventuelles décharges toxiques.
L'allélopathie, également largement utilisée par les algues dans leur lutte pour l’espace contre les coraux, a été abordé dans un précédent article Interactions macro-algues et coraux scléractiniaires. L’arsenal chimique est propre à chaque espèce, on a identifié des sarcophines, des terpénoïdes et des diterpénoïdes en grande quantité et les découvertes ne s’arrêtent pas là. Ces molécules peuvent se combiner entre-elles pour une action synergique ou être dédiées à la lutte contre des prédateurs ciblés. Par exemple, Sinularia flexibilis relargue à des concentrations très faibles une substance terpénique, le flexibilide. Ces substances entrainent l’expulsion de zooxanthelles des coraux durs environnants et le relargage de leurs nématocystes indispensables à la capture de proies. Les tissus meurent et les larves ne peuvent pas non plus s’implanter dans un tel milieu, dans un rayon de cinquante centimètres autour de grandes colonies de coraux cuir Sinularia, Lobophytum et Sarcophyton.
3.5. Écrans solaires internes
La taxinomie chimique consiste à utiliser les métabolites complémentaires, ces substances chimiques spécifiques à chaque espèce, pour leur identification. Elle peut compléter les analyses génétiques et morphologiques des relations au sein des familles. En complément seulement puisque la production de ces métabolites varie en concentration et composition selon les conditions environnementales de manière encore imprécise.
Comme beaucoup d’organismes marins, pour leur protection contre les rayonnements ultraviolets en eaux tropicales claires et peu profondes, les Octocoralliaires métabolisent une famille de composés complexes : les acides aminés de type mycosporine (AAM). Chacun de ces AAM absorbant un rayonnement ultraviolet à une longueur d'onde légèrement différente, ils forment ensemble un écran UV.
3.6. Métabolites complémentaires lors de la reproduction
Le bon déroulement de la reproduction sexuée chez les Octocoralliaires dépend à bien des égards des métabolites complémentaires. Des substances spécifiques, antimicrobiennes et anti-prédation ont été identifiées, comme le pukalide recelé dans les œufs de Sinulariapolydactyla. Le pukalide stimule également la contraction du polype, facilitant la libération des œufs lors de la ponte. D'autres substances incluses dans les œufs agissent comme agents attracitifs spermatiques. Les œufs contiennent également de nombreuses MAA qui assurent la protection UV des larves planctoniques.

3.7. Protections physiques contre les prédateurs
Outre leurs armes chimiques, les Octocoralliaires, disposent de quelques moyens physiques dans leur lutte inter espèces. Ils savent bien sûr rétracter leurs polypes pour se soustraire à une agression, mais leurs spicules calcaires permettent également de repousser quelques envahisseurs. La forme, la taille et le nombre de ces spicules varient selon l’espèce et la zone à protéger : par exemple Silunaria sp, possède des sclérites généralement plus grands et plus nombreux à la base qu’aux extrémités des branches, plus exposées aux poissons prédateurs. Les espèces dont les polypes sont non rétractables et/ou qui possèdent peu de sclérites (Anthelia sp., Xenia sp.), disposent de substances chimiques plus abondantes.
3.8. Protections microbiennes
Le mucus des coraux offre une protection contre les UV, le dessèchement, la sédimentation mais il est colonisé par un large éventail de bactéries, certaines "de passage" et d’autres symbiotiques inféodées au corail. Une bonne proportion contribue à la production de métabolites secondaires, à la protection antifouling contre les salissures marines et à la défense contre d’autres bactéries pathogènes telles que Vibrio. Il a été démontré que la régression de ces bactéries bénéfiques diminue la protection antibiotique et favorise l’apparition de maladies notamment lors des épisodes de blanchissements. Les techniques d’analyses biomoléculaires permettent d’en savoir un peu plus sur l’activité des bactéries associées aux espèces de coraux. Ainsi,la bactérie Pelagiobacter variabilis assure une activité antifouling sur Sarcophyton ; Pseudomonas sp. associée à Sinularia polydactyla ,agit comme antibiotique contre une bactérie pathogène du genre Streptococcus.
4. Agents pathogènes, maladies
Les coraux hébergent de nombreux organismes qui vivent sur ou dans leur hôte à ses dépens. Ces agents infectieux sont pathogènes, ce sont majoritairement des microorganismes comme les virus, bactéries, protozoaires, champignons, des micro à macro-prédateurs comme les vers et arthropodes.
4.1. Modes d'action des agents pathogènes
Virus : un virus est un organisme qui ne dispose pas d'un métabolisme propre il ne peut se reproduire que dans la cellule d'un hôte vivant. Ils peuvent se reproduire dans un organisme sans dommage (comme le rhume ou l’herpès humain) ou se révéler particulièrement destructeur (virus d’Ebola).
Sont dits pathogènes, les agents infectieux (virus, bactéries, champignons ...) qui engendrent des maladies. Ces dernières dépendent à la fois du germe et du terrain sur lequel ils opèrent.
- Pathogènes obligatoires : ils provoquent toujours des maladies. Ils sont spécifiques quand le germe développe une infection caractéristique.
- Pathogènes occasionnels : ils sont inoffensifs dans un porteur sain mais en mesure de développer une maladie en certaines circonstances.
- Pathogènes opportunistes : ils sont habituellement peu agressifs mais peuvent provoquer des troubles chez un hôte affaibli.
Bactéries (Vibrio…) : contrairement au virus, sont autonomes et capables de se reproduire par division cellulaire, pour coloniser l’organisme. De nombreuses bactéries sont bénéfiques et même indispensables et d’autres sont pathogènes. Elles se retransmettent par l'air, l'eau, le sol et les excrétions, le sang, voire transportées par des hôtes-réservoirs pour lesquels elles peuvent être simplement commensales. Les antibiotiques aident à lutter contre ces bactéries pathogènes.
Protozoaires : ce sont de petits animaux, unicellulaires, vivant dans l'eau, les sols humides ou à l'intérieur d'un organisme, bref pratiquement partout. Certains peuvent entraîner des parasitoses dangereuses (paludisme ou maladie du sommeil chez l’homme).
Moisissures : les moisissures pathogènes en milieu marin proviennent de champignons terrestres, dont les spores sont drainés jusqu’à la mer, comme par exemple le genre Aspergillus.
Micro et macro-prédateurs : Parmi les petits parasites ou prédateurs pluricellulaires, on rencontre des vers et des microcrustacés (copépodes). Les copépodes se développent au dépend de leur hôte, fixés sur le tégument (ectoparasites) par des crochets et/ou ventouse, ou plongés dans les cavités gastrovasculaires (endoparasites). Ils se nourrissent directement ou par l’intermédiaire de pièces buccales qui peuvent s'allonger en trompe suceuse ou piqueuse. On trouve des copépodes parasites, de 0,5 à 2 mm, chez tous les cnidaires. Certains appartenant à la famille des Lamippidae sont endoparasitaires des Alcyonacea (Paragorgia…). Les genres Cladiella, Dendronephthya, Heteroxenia, Lemnalia, Litophyton, Lobophytum, Nepthea, Psammogorgia, Sarcophyton, Sinularia, Stereonephthya, Studeriotes, Xenia… hébergent des copépodes qui leurs sont en général associés comme Acanthomolgus, Ansiomolgus, Ascetomolgus, Colobomolgus, Doridicola, Doridicola, Meringomolgus, Monomolgus, Notoxynus, Paradoridicola, Paramolgus, Paredromolgus, Parategastes, Zamolgus… et la liste est encore longue.
4.2. Maladies
Certains germes sont toujours présents dans l’hôte et ne peuvent vivre ailleurs, d’autres vivent dans des environnements très variés, en dehors ou à l’intérieur de l’hôte. Les maladies et les modes d’action des germes qui les rendent subitement dangereux, sont encore mal connus. Ces dernières années, les chercheurs qui les étudient de près en raison de leur impact sur l'avenir des récifs coralliens, ont découvert de nombreux pathogènes et ils reconsidèrent sans cesse ceux, agissant seuls, en associations ou en successions, qui sont réellement à l’origine des maladies. Les désagréments environnementaux, la pression de l’homme… génèrent des stress qui rendent les coraux plus sensibles aux envahisseurs et à ces pathogènes. L’état de santé des colonies commence depuis peu à faire l’objet de suivis, c’est une étape indispensable pour mieux les comprendre et mettre en place des programmes de conservation des récifs coralliens.
On a pu répertorier une dizaine de maladies sur les coraux. Certaines comme l’Aspergillose sont spécifiques aux Octocoralliaires, d’autres n’ont été observées aujourd’hui que sur des Hexacoralliaires, mais qu’en sera-t-il demain ? Le tableau ci-après les répertorie toutes, à titre d’information.
| Maladie | Observations | |
|---|---|---|
|
Blanchissement Bleaching 
|
Description | Le blanchissement se traduit par une perte de couleur partielle ou généralisée de l’animal, les tissus s'éclaircissent, deviennent pâles jusqu'à transparents. Les coraux peuvent alors présenter des colorations fluorescentes jaune ou vert pâle. À l'extrême, le squelette se dénude totalement et devient d'un blanc pur. |
| Pathogène | Vibrio shiloi, V. coralliilyticus... | |
| Pathogénèse | Facteurs incriminés : il peut s’agir d’un symptôme commun en réponse à des agressions différentes, aussi bien d'origine biotique qu'abiotique. - Blanchissement "classique" : Il apparaît comme une réponse généralisée face à un stress dû à des agressions environnementales : des températures extrêmes (supérieures de 2°C à la moyenne) seraient le facteur prépondérant et variable selon la tolérance de l'espèce ; une irradiation lumineuse trop forte ou inappropriée ; des périodes d’obscurité prolongées ; une baisse de la salinité ; la présence de métaux lourds (cadmium) ; des carence en sels nutritifs. Face à ce stress oxydant induit par un dérèglement de la photosynthèse (photoinhibition), le corail se sépare de ses zooxanthelles (devenues toxiques) afin de maximiser ses chances de survie. Il peut survivre quelques semaines et, si les conditions environnementales se rétablissent, être recolonisé par les zooxanthelles. En cas de prolongement, la symbiose avec les algues n'est pas rétablie, le corail ne s'alimente plus par photosynthèse, finit par nécroser et mourir. - Blanchissement bactérien : plus récemment, des scientifiques contestent la thèse des perturbations environnementales et revendiquent celle de la maladie dont les pathogènes seraient des bactéries (Vibrio shiloi, V. coralliilyticus), des virus ou des parasites (coccidies). |
|
| Cas concernés | Scléractiniaires et Octocoralliaires symbiotiques ainsi que tous les autres organismes marins qui vivent en relation avec des algues symbiotiques, dans toutes les mers. Les Octocoralliaires semblent mieux résister, dans la majorité des cas, aux élévations de température que les Scléractiniaires. | |
| Traitements | En aquarium, rétablir le facteur de maintenance à l'origine du stress, à un niveau acceptable pour l'espèce concernée (température, éclairage, toxines...). | |
|
Maladie des bandes noires Black band desease (BBD) 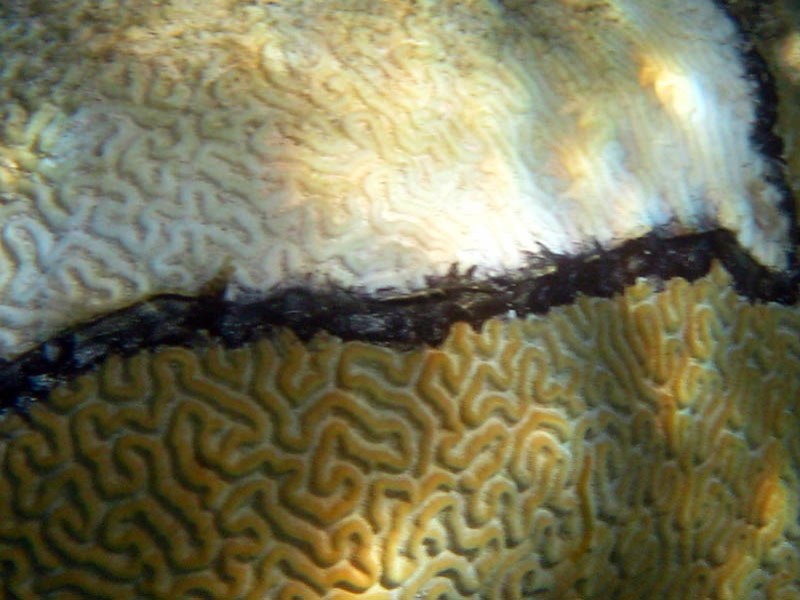 |
Description | Présence d’une bande noire à la surface du tissu, assez mate de quelques millimètres à quelques centimètres de largeur, entre des zones saines. Propagation de quelques millimètres par jour mettant le squelette à nu et pouvant anéantir une colonie en moins d’un mois. On ne note pas de changements de couleur ou de morphologie du tissu du corail. Le phénomène peut s’arrêter, la bande noire disparaît et le tissu non détruit reprend sa croissance et, selon l'espèce, peut recouvrir la partie du squelette dénudé. La partie morte est parfois colonisée par des algues à l’origine de l’étouffement du reste de la colonie. |
| Pathogène | La cyanobactérie filamenteuse Phormidium corallyticum semble à l’origine de la coloration noire (elle contient un pigment photosynthétique, phycoérythrine, rouge en grande quantité) . D’autres bactéries Spirulina sp. et Beggiatoa, fréquemment identifiées au niveau de la bande noire, semblent jouer un rôle secondaire. | |
| Pathogénèse | Certains facteurs augmentent l’incidence et la prévalence de la maladie : sédiments, toxiques chimiques produits par des algues, élévation de température > 26°C, variation de salinité. Le tissu du corail est détruit en raison de l’absence d’oxygène au contact de la bande noire et à son exposition au sulfure d’hydrogène produit par les bactéries. Le squelette du corail laissé derrière est alors en contraste avec la bande noire créée par les cyanobactéries |
|
| Cas concernés | Scléractiniaires (Faviidés), et quelques Octocoralliaires Sinularia sp., et gorgones, essentiellement de Mer Rouge et de l'océan Indopacifique. Tubipora musica et les Fungiidés semblent immunisés. | |
| Traitements | Traitement antibiotique à base de sulfate de néomycine. Possibilité de retirer les tissus nécrosés et cautériser à la résine époxy. | |
|
Aspergillose Aspergillosis (ASP) 
|
Description | Une ou plusieurs taches irrégulières ou une perte extensive de tissus, pourpre, avec de fins filaments blancs et des sédiments le long de la structure axiale. Souvent les tissus adjacents aux taches présentent une coloration plus intense |
| Pathogène | Mycose due au champignon terrestre Aspergillosus sydowii, introduit par l'érosion des sols. | |
| Pathogénèse | Dans certaines conditions, les spores germent à la surface du corail, puis l’hyphe du champignon pénètre à l’intérieur des tissus, entraînant ainsi sa mort. La gorgone sécrète alors de la mélamine (responsable de la couleur pourpre) pour isoler la zone infectée. | |
| Cas concernés | Observée sur des Octocoralliaires aux Caraïbes, Bahamas, République Dominicaine, Floride, Jamaïque et Antilles, notamment sur les deux gorgones Gorgonia flabellum et G. ventalina. | |
|
Gelée brune Brown jelly syndrome (BJS) 
|
Description | Nécrose des tissus avec une masse gélatineuse brune en arrière des zones encore saines. L’avancée peut atteindre plusieurs centimètres par jour sur un Alcyonaire. Dans des conditions naturelles, l’action des vagues éliminerait la gelée, seul le front de nécrose serait visible |
| Pathogène | Observation de nombreux protozoaires opportunistes principalement Helicostoma nonatum, ainsi que de petits vers et copépodes. | |
| Pathogénèse | Des bactéries ou des blessures sont à l’origine de l’infection ; il s’ensuit un développement rapide des protozoaires qui ingèrent une grande quantité de zooxanthelles ; leur action est complétée par celle de vers et de copépodes qui semblent être opportunistes. L'infection est contagieuse et se développe d'autant plus vite que la température est élevée et l'eau riche en nutriments. | |
| Cas concernés | Scléractiniaires, notamment Euphyllia, Goniopora et Acropora et Octocoralliaires, principalement Nephtéidés, Anthelia, Cladiella et Xenia. Touche aussi les anémones coloniales (Zoanthus, Palythoa, Parazoanthus). Observé uniquement en aquarium | |
| Traitements | Retirer les zones infectées. Traitement aux antibiotiques tels que métronidazole (également contre les protozoaires). | |
|
Maladie de la bande rouge Red band disease (RBD) 
|
Description | Ressemble à la maladie de la bande noire. La bande présente une couleur rouge brique ou marron foncé, avec de part et d'autre une zone saine et une zone blanche. La progression semble assez lente |
| Pathogène | Probablement cyanobactérie | |
| Pathogénèse | La bande rouge est composée de cyanobactéries et de microorganismes différents de ceux retrouvés dans la maladie de la bande noire. On pense, à l’heure actuelle, que les microorganismes sont différents selon les types de coraux | |
| Cas concernés | Scléractiniaires essentiellement ceux de formes massive ou en plateau (Diploria, Montastraea, Porites, Siderastrea, Colpophyllia) et Octocoralliaires essentiellement les gorgones. Peu fréquente, observée aux Caraïbes et sur la Grande barrière de corail. | |
| Traitements | Peut-être par antibiotique à base de sulfate de néomycine. Possibilité de retirer les tissus nécrosés et cautériser à la résine époxy. | |
|
Anomalies de développement Growth Anomalies (GAs) 
|
Description | Le corail pousse plus rapidement formant des reliefs aberrants : excroissances des tissus (néoplasies) ou augmentation du volume des tissus (hyperplasie). Le squelette est dans ces zones, moins dense. |
| Pathogène | Causes multiples non identifiées. | |
| Pathogénèse | Il a été observé dans les tissus des hyphes de champignon, associées à une perte locale de symbiotes. On suggère que des causes environnementales perturbent la croissance en même temps qu'elles rendent le corail plus sensible aux pathogènes. | |
| Cas concernés | Scléractiniaires (Acropora palmata, Platygyra, Porites) et Octocoralliaires (gorgones), notamment Pseudoplexaura, Gorgonia ventalina. | |
|
Maladie de la bande blanche (régression tissulaire) White band desease (WBD) 
|
Description | Une bande blanche précède le tissu sain. Les tissus reculent de façon uniforme à une vitesse constante de quelques millimètres par jour, à partir de la base de la colonie, pèlent puis se détachent, laissant ainsi apparaître le squelette blanc du corail. La partie mise à nu du squelette peut être colonisée par des algues (Ostreobium sp) et peut apparaître verdâtre. Le tissu remanié ne présente pas de signe de blanchiment. Il existe une forme un peu différente où on constate un blanchiment du tissu en aval de la zone dénudée. La maladie débute à la base du corail (ou au milieu des branches) et se dirige vers l’extrémité des branches. |
| Pathogène | Origine inconnue. On a trouvé dans certains cas des bactéries à Gram négative dont Vibrio charcharii sans pouvoir affirmer que ce sont des pathogènes. | |
| Pathogénèse | Inconnue, la maladie serait une réponse à un stress | |
| Cas concernés | Scléractiniaires, essentiellement Acropora et parfois Platygyra et Hydnophora. Observée aux Caraïbes, Philippines, Grande barrière de corail, mer Rouge et Bahamas. | |
| Traitements | La maladie est insensible aux antibiotiques. Retirer les portions infectées, un bain de lugol peut limiter la prolifération. Améliorer les conditions de maintenance. | |
|
Peste blanche White plague (WP) 
|
Description | Semblable en apparence à maladie de la bande blanche, mais elle affecte différentes espèces et plus particulièrement les colonies massives et encroûtantes. La maladie est caractérisée par une ligne ou bande qui sépare brusquement les tissus vivants du squelette colonisé par les algues. Souvent une étroite bande de tissu blanchi peut être visible du côté du squelette exposé. Elle commence habituellement à la base d'une colonie et se propage rapidement vers le haut et l'extérieur |
| Pathogène | Suspicion de bactéries Aurantimonas coralicida et Sphingomonas sp. et plus récemment, identification d'un virus. | |
| Pathogénèse | Très rapide, de petites colonies peuvent être décimée en un à deux jours. Trente-deux espèces sont touchées. | |
| Cas concernés | Scléractiniaires. Détectée dans les Caraïbes notamment sur Dichocoenia stockesii. Non connue en aquarium |
Maladie des plages blanches White patch desease (WPD) 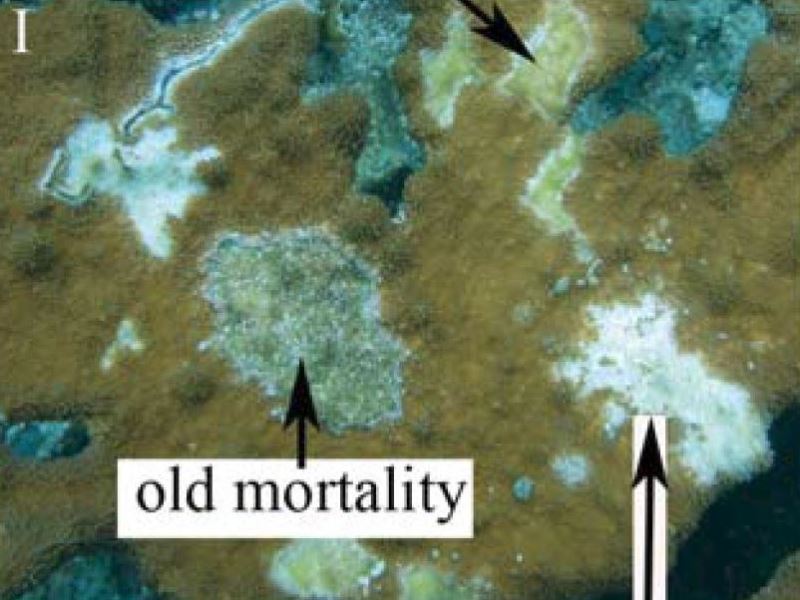
|
Description | Perte massive, partielle ou totale, de tissus laissant apparaître le squelette. La progression est rapide environ 2 cm/j à très rapide 10 cm/j et la mortalité très importante et peu toucher la totalité de la colonie |
| Pathogène | Certaines formes de la maladie seraient dues à une bactérie Gram négatif, aérobie stricte et hétérotrophe Aurantimonas coralicida, | |
| Pathogénèse | Inconnue. | |
| Cas concernés | Scléractiniaires, les espèces massives, incrustantes et branchues sont les plus touchées | |
|
Maladie des bandes Jaunes Yellow band desease (YBD) 
|
Description | Nécrose laissant apparaître autour de la partie centrale dénudée du corail, une bande concentrique de tissu de couleur jaune pâle, d’de largeur comprise entre 1 et 10 cm. Le squelette dénudé peut parfois rester de couleur jaune et peut également être envahi par des algues. La progression est rapide et dépend des conditions du milieu, notamment de la température. |
| Pathogène | Bactérie Vibrio spp. suspectée. | |
| Pathogénèse | Similaire à la maladie de la bande noire. | |
| Cas concernés | Scléractiniaires, surtout les formes massives. Fréquente sur Acropora, mais aussi certains Cyphastrea, Porites, Turbinaria reniformis. Observée en Floride, Caraïbes et golf Arabique | |
| Traitements | Ablation des zones infectées. | |
|
Nécrose rapide des tissus Rapid tissues necrosis (RTN) 
|
Description | Dégradation fulgurante des tissus mettant à nu le squelette du corail. Elle touche simultanément l’ensemble des branches ou bien se propage de branche en branche de plusieurs centimètres par jour. Maladie très contagieuse qui peut anéantir en quelques jours la totalité des coraux d’un aquarium. |
| Pathogène | Les bactéries Vibrio harveyi, V. vulnificus on été observées sans certitude sur leur caractère pathogène. | |
| Pathogénèse | L'origine pourrait être bactérienne ou virale. Le fait que des RTN se sont déclarées sans observation de micro-organisme, laisse penser que la maladie consisterait en une forme d'autolyse du corail, liée à un stress environnemental entretenu par des microbes opportunistes. | |
| Cas concernés | Scléractiniaires. | |
| Traitements | Préventivement, observer une quarantaine à l'acquisition. La RTN étant déclarée, agir très rapidement pour éviter la contagion. Retirer les colonies infectées à l'écart dans un bain et tailler les zones infectées. Il a été signalé une limitation de la contagion sous UV ou Ozone. Un traitement au chloramphénicol entre des bains de lugol a été préconisé sans garantie sur son efficacité absolue. | |
5. Parasites et prédateurs
5.1. Planaires

Les planaires sont les plus connus des vers plats et mous de l'embranchement Plathelminthes et de la classe Turbellaria. Les planaires sont libres ou rampantes, aplaties ventrodorsalement, de forme arrondie plus ou moins allongée et la queue parfois fourchue. Leur longueur varie selon l’espèce, de quelques millimètres à plusieurs centimètres, leur épaisseur ne dépassant pas un à deux millimètres. Leur teinte varie de gris clair à brun avec souvent une bande dorsale. Hermaphrodites synchrones (successivement mâles et puis femelle), les planaires se reproduisent essentiellement de manière sexuée par fécondation croisée des unes et des autres, et de manière asexuée par scissiparité bilatérale. L’article Coraux durs et invertébrés parasitaires, traite dans le détail du mode d’action des planaires et des nudibranches. Bien que n'étant pas pathogènes, mais toujours présentes sur leurs hôtes, elles représentent un danger pour les coraux. Les Octocoralliaires sont surtout la cible des planaires du genre Waminoa. Ces parasites opportunistes semblent procéder de différentes manières, plus ou moins complémentaires, pour nuire, jusqu’à provoquer la mort de leur hôte : ils subtilisent le plancton capté par le corail (cleptoparasitisme), immobilisent sa bouche et se nourrissent de son mucus (Dendronephthya, Stereonephthya…), ou prolifèrent jusqu’à former un écran empêchant la photosynthèse des algues symbiotiques des espèces zooxanthellées (Sarcophyton, Sinularia, Xenia…).
5.2. Mollusques : gastéropodes et nudibranches

Cet embranchement comprend de nombreuses espèces parasites et prédatrices. Ce sont essentiellement des gastéropodes et nudibranches.
Parmi les gastéropodes consommateurs de polypes, on peut citer : Heliacus aerola, Philipia sp. Architectonica sp. Jenneria sp. Drupa sp. Drupella cornus (murex), Rapa rapa, Coralliophila sp., Leptoconchus sp. Magilopsis sp. Magilus sp., Epitonium sp. Quelques-uns sont associés à certaines espèces. Les gastéropodes de la famille des Ovulidae s’attaquent essentiellement aux coraux mous et aux gorgones. Les principaux ovules parasites sont : Volva brevirostris, Prionovolva sp., Simnia loebbeckeana, Ovula ovum, Diminovula sp. La porcelaine Cyphoma gibbosum (langue de flamant), fréquemment vendue en magasin aquariophile affectionne particulièrement les gorgones zooxanthellées Plexaurella spp., Gorgonia ventalina et G. flabellum mais en leur absence pourra se contenter d’autres espèces.
Les nudibranches ont en général un régime alimentaire spécialisé et s’attaquent spécifiquement à un genre de corail, avec lequel ils présentent un mimétisme prononcé. Parmi ceux qui affectionnent les Octocoralliaires, citons : Phylliodesmum sp., Dendronotus sp., Marionopsis sp. et Tritonopsilla sp. Tritonia sp. et Tritoniopsis se nourrissent des gorgones Pseudopterogorgia spp. et Gorgonia spp. mais génèrent peu de dommages tant que leur population n’est pas trop envahissante, cependant les polypes restent rétractés en leur présence.

5.3. Annélides polychètes
Ces vers prédateurs errants, dont la taille varie de quelques millimètres à plusieurs centimètres, possèdent des soies plus ou moins nombreuses et de taille variable. Ils disposent d’une trompe dévaginable pourvue de puissantes mâchoires chitineuses. Leur action prédatrice s’exerce par taraudage, par ingestion de polypes ou encore par perforation des coraux. Le ver de feu Hermodice carunculata, bien connu des aquariophiles s’attaque aux coraux scléractiniaires, aux anémones mais aussi aux Octocoralliaires.
5.4. Crustacés
La nuisance provient essentiellement de crevettes : Saron marmotus (crevette « marbrée »), Saron inermis, Rhynchocinetes uritai (crevette à bosse). Corallivores, elles exercent une prédation sur les coraux.
5.5. Etoiles de mer
Acanthaster planci, cette grosse étoile de mer épineuse, nommée « Coussin de belle-mère », est corallivore au stade adulte. Son régime n’est pas strict il est orienté sur les Scléractiniaires mais elle ne dédaigne pas les Octocoralliaires (gorgones et Alcyonaires) ainsi que les algues. Elle dévagine alors son estomac et l’applique sur les polypes qu’elle digère sur place avant de le rétracter. Une Acanthaster planci peut détruire 5 à 6 m² de corail par an, une colonie peut donc éradiquer plusieurs km² par an.
5.6. Poissons corallivores
Les coraux ont su développer des moyens de défense, mais ils ne sont pas épargnés par les quelques 130 espèces de poissons corallivores : Chaetodonidés, Balistidés, Monacanthidés (poissons limes), Ostracionidés (poissons coffres), Tetraodontidés (canthigaster, arothron)... Les Scléractiniaires sont les plus touchés mais si les Octocoralliaires sont particulièrement doués dans la production de substances chimiques répulsives, ils ne sont pas à l’abri.

Ces poissons coralliens ont développé de nombreux modes d’alimentation pour exploiter la manne proposée par le récif. Il existe des consommateurs de polypes et tissus des coraux ; la prédation des poissons-papillons sur certains SPS peut représenter jusqu’à 6 % de leur biomasse par an, soit un besoin énergétique important pour leur reconstitution et un impact non négligeable sur la répartition et l’abondance des communautés concernées. Bien qu’il soit difficile d’identifier la nature de la nourriture consommée par les corallivores, il est avéré qu’ils consomment tout autant le mucus des coraux, c’est le cas de Labrichthys unilineatus. Les consommateurs de squelettes qui créent de grands dommages sur les tissus, concernent bien évidemment les scléractiniaires. Les poissons peuvent également endommager les colonies en se nourrissant des microorganismes qui s’y réfugient.
Un tiers de ces prédateurs, corallivores stricts, se sont spécialisés sur des genres spécifiques. Les Chaetodontinés (poissons-papillons) représentent la moitié des espèces prédatrices, ils sont friands de gorgones, certains comme Chaetodon melannotus préfèrent cependant les Alcyonnaires. En captivité, la pression des poissons-papillons est en général trop forte pour les coraux hébergés. Les espèces sont le plus souvent des corallivores facultatifs : s’ils ne dédaignent pas grignoter des polypes, ils consommeront d’autres nourritures, comme les poissons-anges qui consomment polypes et tissus de gorgones ou des colonies d’Alcyons, mais aussi les éponges ou les Tetraodontidés
La prédation par les corallivores n’est pas le seul effet sur la santé des coraux. On a pu observer que les poissons pouvaient être vecteurs de maladies, propageant des germes d’une colonie à une autre. À contrario, certaines espèces sont en mesure de nettoyer les tissus infectés, comme lors de la maladie de la bande noire, ralentissant ainsi sa progression.
Références
- K. Fabricius, P. Alderslade. Soft corals and sea fans – A comprehensive guide to the tropical shallow-water genera of the Central-West Pacific, the Indian Ocean and the Red Sea. Australian Institute of Marine Science, Townsville, Australia. 2001. 264 p
- J. Sprung, J. C. Delbeck. L’aquarium récifal, volume 2. Ricordea Publishing 1999.
- A. Bruckner. Field Guide to Western Atlantic Coral Diseases and Other Causes of Coral Mortality. 2009.
- T. V. Raveendran, V. P. Limna Mol. Natural product antifoulants. National Institute of Oceanography, Council of Scientific and Industrial Research. Kochi, India. Current Science, vol. 97, n°. 4, 25 august 2009.
- NOAA Fisheries. Coral Reef Ecosystem Division's field assessment of Indo-Pacific coral diseases and compromised health states - Overview of Coral and Algal Diseases. National Oceanic and Atmospheric Administration (NOAA) Fisheries.
- E. Rosenberg, Y. Loya Coral. Corals Health and Disease. Springer Science & Business Media, avril 2004 - 488 pages.
- Major Reef-building Coral Diseases. NOAA's Coral Reef Information System (CoRIS)
- Aquarium Coral Diseases website du Dr Michael Sweet, researcher in the Coral Health and Disease Laboratory at Derby University, UK.
- Disease In Tropical Coral Reef Ecosystems. ICRI/UNEP-WCMC (2010).
- Underwater Cards for Assessing Coral Health on Caribbean Reefs. Coral Reef Targeted Research
- D. Riddle. Parasitic Copepods: Enemies of Soft Corals, False Corals, Gorgonians, Anemones, Zoanthids, and Tridacna Clams. Advanced Aquarist, volume IX, avril 2010.
- T. Wijgerde. Epizoic flatworms impair coral feeding: evidence for parasitism. Advanced Aquarist, volume XI, novembre 2012.
- Kim B. Ritchie. Regulation of microbial populations by coral surface mucus and mucus-associated bacteria. MARINEMarine Ecology Progress Series. Vol. 322: 1–14, 2006.
- J. KERRY. Relationship between corals and fishes on the Great Barrier Reef. Australia’s Tropical Land and Seas.
Tous mes remerciements aux auteurs des photos pour leur accord de publication et à mes correcteurs Christian SEITZ, Olivier SOULAT et Jérémie VIDAL DUPIOL, pour leur soutien.
Denis TOURNASSAT
Article publié par Cap récifal le 04 janvier 2015 avec l'aimable autorisation de l'auteur.
Modifié par Denisio


Commentaires recommandés
Il n’y a aucun commentaire à afficher.